1. Pozadí epidemie dengue: Eskalace globální výzvy v oblasti veřejného zdraví
Dengue je akutní virové onemocnění přenášené komáry způsobené virem dengue (DENV), který se stal celosvětově nejrychleji se šířícím arbovirovým onemocněním a představuje značnou hrozbu pro veřejné zdraví. Během posledních dvou desetiletí se celosvětový výskyt dengue dramaticky zvýšil a počet hlášených případů se od roku 2021 každoročně zdvojnásobuje [1]. V prosinci 2023 Světová zdravotnická organizace (WHO) vyhlásila globální stav nouze v souvislosti s dengue, aby posílila koordinované mezinárodní úsilí v oblasti reakce. Epidemiologické odhady WHO ukazují, že přibližně 3,9 miliardy lidí na celém světě je ohroženo nákazou dengue, přičemž ročně dochází k odhadovaným 390 milionům infekcí – z nichž 96 milionů se projeví jako klinicky zjevné případy [1,2].
2 epidemiologické hlavní body
Epidemiologické charakteristiky horečky dengue jsou formovány interakcí virologických faktorů, ekologie vektorů, imunitních reakcí hostitele a socioenvironmentálních podmínek. Komplexní pochopení těchto charakteristik je nezbytné pro vývoj účinných strategií prevence a kontroly, jakož i přesných diagnostických přístupů.
2.1 Vektory přenosu a vzorce přenosu ve městech
Virus dengue se přenáší primárněAedes aegypti a Aedes albopictuskomáři. Mezi těmito druhy přenašečů je Aedes aegypti považován za nejvýznamnějšího přenašeče, který se vyznačuje vysokou „adaptabilitou pro člověka“ a širokým rozšířením v tropickém a subtropickém městském prostředí. Na rozdíl od jiných komárů přenašečů arbovirových patogenů vykazuje Aedes aegypti následující klíčové epidemiologické charakteristiky:
-Preference pro rozmnožování v antropogenním prostředí (např. nádoby na vodu, vyřazené pneumatiky)
-Silný tropismus pro lidskou krev jako zdroj živin
-Denní krmné chování
Tyto znaky definují horečku dengue jako typické onemocnění„městská infekční nemoc“,s výrazně zvýšenou účinností přenosu v hustě osídlených oblastech. Studie související s WHO prokázaly, že v hustě osídlených městských prostředích může zvýšená frekvence kontaktu komárů s člověkem podstatně zvýšit základní reprodukční číslo (R₀) viru DENV, a tím urychlit šíření epidemií [2].
2.2 Globální trendy spreadu a jejich hnací faktory
Podle zpráv WHO se celosvětový počet hlášených případů dengue za poslední dvě desetiletí exponenciálně zvýšil [1,3]. Tento vzestupný trend je primárně způsoben následujícími vzájemně propojenými faktory:
(1) Změna klimatu: Rostoucí globální teploty nejen rozšiřují geografický rozsah vhodných stanovišť pro komáry přenašeče, ale také zkracují vnější inkubační dobu DENV v hostiteli komára, čímž zvyšují účinnost přenosu. Klimaticky vyvolané změny v hustotě komárů byly WHO ověřeny jako spolehlivý prediktor časoprostorové dynamiky ohnisek dengue.
(2) Urbanizace: Rychlá a neplánovaná expanze měst vytvořila hojná místa pro rozmnožování komárů přenašečů, zatímco zvýšená hustota obyvatelstva posílila kontinuitu přenosových řetězců DENV.
(3) Globální pohyb obyvatelstva: Mezinárodní cestování a obchod usnadnily rychlý přeshraniční přenos dengue a podpořily přechod od importovaných případů k trvalému lokálnímu přenosu. Data ze sledování WHO ukazují, že mezi lety 2010 a 2021 Spojené státy hlásily 7 528 případů dengue souvisejících s cestováním, z nichž 3 135 vyžadovalo hospitalizaci a 19 mělo za následek úmrtí.
(4) Rozšíření rozšíření přenašečů: Celosvětově se geografický areál rozšíření Aedes aegypti a Aedes albopictus nadále rozšiřuje a komáři rodu Aedes se stále více usazují v některých částech Evropy. V důsledku toho se horečka dengue vyvinula z tradičně regionální epidemie v globální hrozbu pro veřejné zdraví.
2.3 Mechanismy multiserotypové ko-cirkulace a reinfekce
Virus dengue se skládá ze čtyř antigenně odlišných sérotypů (DENV-1 až DENV-4). Infekce jedním sérotypem poskytuje dlouhodobou ochrannou imunitu proti tomuto specifickému sérotypu, ale pouze dočasnou a částečnou zkříženou ochranu proti ostatním třem sérotypům. Běžná populace je všeobecně náchylná k DENV, přičemž klinické onemocnění se vyvine pouze u podskupiny infikovaných jedinců [2].
V endemických oblastech často cirkuluje současně více sérotypů viru dengue, což vede k tomu, že jedinci mohou během svého života prožít více infekcí dengue. Epidemiologické studie WHO identifikovaly kocirkulaci více sérotypů jako klíčový faktor periodických propuknutí dengue [1].
2.4 Sekundární infekce a zesílení závislé na protilátkách
Kritickým a jedinečným jevem v epidemiologii dengue jeprotilátkově závislé zesílení (ADE)Během sekundární infekce heterologním sérotypem DENV usnadňují neneutralizující protilátky produkované během primární infekce vstup viru do monocytů a makrofágů, čímž zvyšují replikaci viru. Tento mechanismus je WHO široce uznáván jako hlavní patogenní faktor u těžké formy dengue, včetně hemoragické horečky dengue a šokového syndromu dengue [1].
Epidemiologická data WHO důsledně ukazují, že jedinci se sekundární infekcí dengue mají výrazně vyšší riziko vzniku závažného onemocnění ve srovnání s osobami s primární infekcí – což je charakteristika, která má velký význam pro sledování onemocnění a klinickou léčbu. Je důležité poznamenat, že zatímco riziko závažného onemocnění je během sekundární infekce zvýšené, infekce jakýmkoli sérotypem DENV může potenciálně vyvinout závažnou formu dengue [1].
2.5 Nespecifické klinické projevy a riziko chybné diagnózy
Klinické projevy horečky dengue jsou pozoruhodně nespecifické, zejména v raných stádiích onemocnění, a často se překrývají s projevy jiných virových infekcí přenášených komáry (např. viry chikungunya a Zika) a také s některými respiračními infekcemi. Odhady WHO uvádějí, že 40–80 % infekcí dengue je asymptomatických [3].
Mezi typické klinické projevy patří:
-Akutní horečka (přetrvávající 2–7 dní, která může být dvoufázová)
- Silná bolest hlavy a retroorbitální bolest (bolest za očima)
-Bolest svalů a kloubů (běžně označovaná jako „horečka zlomených kostí“)
-Makulární nebo makulopapulární vyrážka
- Mírné hemoragické projevy (např. ekchymóza, epistaxe, krvácení dásní)
Symptomatická dengue se obvykle dělí do tří odlišných fází: horečnaté fáze, kritické fáze a fáze zotavení. Přibližně méně než 5 % symptomatických pacientů progreduje do těžké dengue. Vzhledem k nedostatku specifických klinických znaků je diagnóza založená pouze na klinických příznacích obtížná, což zvyšuje riziko chybné diagnózy a poddiagnostiky. WHO výslovně zdůrazňuje, že samotná klinická diagnóza nestačí k zajištění přesnosti, a proto je laboratorní potvrzení nezbytné [1].
3 klíčové body z dokumentu WHO „Laboratorní testování viru dengue: Prozatímní pokyny, duben 2025“
V dubnu 2025 vydala Světová zdravotnická organizace aktualizované prozatímní pokyny pro laboratorní testování na dengue (DENV), které poskytují směrodatné technické pokyny pro globální diagnostiku dengue. Tyto pokyny syntetizují nejnovější důkazy o laboratorním testování dengue v kontextu probíhající globální nouzové situace v souvislosti s dengue a nabízejí praktická doporučení přizpůsobená prostředím s různou úrovní zdrojů.

3.1 Základní principy testovací strategie
Pokyny zdůrazňují, že diagnostika horečky dengue musí využívat strategii kombinovaného testování s využitím více markerů na základě stádia onemocnění [1]. Vzhledem k absenci univerzálního diagnostického algoritmu by testovací strategie měly být přizpůsobeny místním epidemiologickým kontextům s ohledem na následující klíčové faktory [1]:
-Stádium infekce: Počet dní po nástupu příznaků určuje nejvhodnější testovací metodu
-Typ vzorku: Vhodnost plné krve, plazmy nebo séra pro detekci DENV
-Regionální epidemiologie: Lokálně cirkulující sérotypy DENV a společná cirkulace jiných arbovirů
-Riziko koinfekce: V oblastech s překrývající se cirkulací arbovirů by se mělo zvážit multiplexní testování k rozlišení mezi různými patogeny.
3.2 Strategie testování založená na fázích
Podle pokynů WHO by laboratorní testování na horečku dengue mělo dodržovat jasná časová okna založená na stádiu onemocnění [1,2]:
(1) Testování akutní fáze (≤7 dní po nástupu)
-Testování nukleových kyselin (molekulární testování): Reverzní transkripce-polymerázová řetězová reakce (RT-PCR) a další molekulární metody detekují RNA DENV s vysokou citlivostí.
-Testování antigenu: Detekce antigenu NS1, který se stává detekovatelným během 1–3 dnů po nástupu onemocnění.
Během akutní fáze jsou hladiny virémie relativně vysoké a testování nukleových kyselin a antigenů dosahuje optimální citlivosti.
(2) Testování v rekonvalescenční fázi (≥4 dny po nástupu onemocnění)
-Sérologické testování: Protilátky IgM jsou obvykle detekovatelné kolem 4. dne po nástupu onemocnění.
Ve většině případů přetrvávají protilátky IgM 14–20 dní a v některých případech může perzistence trvat až 90 dní.
Testování IgG má omezenou hodnotu pro diagnózu akutní horečky dengue kvůli možné zkřížené reakci protilátek z předchozí infekce flavivirem nebo očkování.
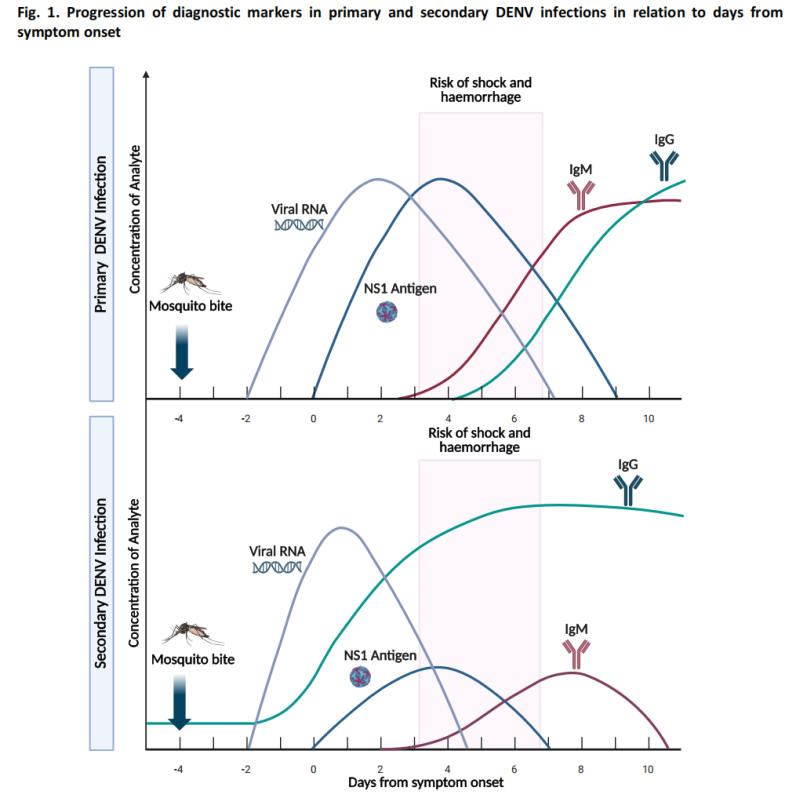
(3) Diagnostický algoritmus pro podezřelé případy
Pokyny zahrnují diagnostický algoritmus pro podezření na horečku dengue a doporučují vhodné testovací metody na základě počtu dnů po nástupu příznaků: testování antigenu NS1 a testování nukleových kyselin jsou primárními přístupy v rané fázi, zatímco sérologické testování je primární metodou v pozdější fázi.
3.3 Hodnocení a výběr výkonnosti zkušební metody
Podle WHO je systematické hodnocení výkonnosti a použitelných scénářů různých testů na horečku dengue následující:
| Testovací metoda | Cíl | Časové okno | Primární scénář aplikace | Úvahy |
| Testování nukleových kyselin | Virová RNA | 1–7 dní po nástupu | Včasné potvrzení, identifikace sérotypu | Zlatý standard; vyžaduje specializované laboratorní vybavení a technické znalosti |
| Testování antigenu NS1 | Nestrukturální protein | 1–3 dny po nástupu | Včasný rychlý screening | K dispozici ve formátu rychlého diagnostického testu (RDT), vhodného pro prostředí s omezenými zdroji |
| Testování protilátek IgM | Specifické protilátky IgM | ≥4 dny po nástupu | Diagnóza nedávné infekce | Jediný odběr séra naznačuje pouze možnou nedávnou infekci; k potvrzení je nutná sérokonverze. |
| Testování protilátek IgG | Specifické protilátky IgG | Rekonvalescentní/předchozí infekce | Epidemiologické vyšetření, posouzení stavu imunity | Jeden vzorek séra není vhodný pro diagnózu akutní horečky dengue. |
| Kombinované testování (NS1+IgM/IgG) | Antigen + protilátky | Úplný průběh onemocnění | Komplexní diagnostika infekce horečkou dengue | V současné době nejvýkonnější formát RDT pro diagnostiku horečky dengue |
| NGS | Virová RNA | 1–7 dní po nástupu | Virový genomický dohled | Vyžaduje specializované sekvenční vybavení a schopnosti bioinformatické analýzy |
4 Doporučení produktů pro detekci horečky dengue pomocí makro a mikro testů podle scénáře
Pro podporu prevence a kontroly horečky dengue poskytuje Macro & Micro-Test integrované diagnostické portfolio zahrnující rychlý screening, molekulární potvrzení a genomický dohled, a splňuje tak potřeby v různých fázích zvládání epidemie.
4.1 Scénář 1: Rychlý screening a cílený dohled
Platí pro kliniky pro léčbu horečky, zařízení primární zdravotní péče, screening komunit v době ohniska a karanténu v přístavech/na hranicích.
-Rychlý test na antigen viru dengue NS1: Detekuje časnou infekci (1–3 dny po nástupu) s výsledky do 15 minut pro rychlé třídění.
-Test protilátek IgM/IgG proti viru dengue: Rozlišuje primární a sekundární infekce pro vyhodnocení rizika závažného onemocnění.
Kombinovaný rychlý test na antigen NS1 viru dengue + IgM/IgG: Současně detekuje antigen a protilátky pro kompletní diagnózu.
-Test protilátek IgM/IgG proti viru chikungunya: Umožňuje diferenciální diagnostiku s horečkou dengue a přesnou identifikaci patogenů.
4.2 Scénář 2: Přesná diagnostika a reakce na mimořádné události
-Souprava pro detekci nukleových kyselin viru dengue I/II/III/IV: Detekuje a diferencuje 4 sérotypy (detekční limit 500 kopií/ml) pro sledování ohnisek nákazy.
-Lyofilizovaná PCR sada pro virus dengue: Přenosná při pokojové teplotě, vhodná pro oblasti s omezenými zdroji a náhlá ohniska.
-Sada pro multiplexní PCR v reálném čase pro detekci horeček dengue/ziky/chikungunya: Současně detekuje 3 arboviry pro efektivní diferenciální diagnostiku komplexních epidemií.

Všechny výše uvedené reagencie jsou kompatibilní s plně automatizovaným systémem AIO 800 Sample-to-Answer, což snižuje manuální obsluhu a křížovou kontaminaci a zvyšuje efektivitu a biologickou bezpečnost.
4.3 Scénář 3: Genomický dohled a analýza virové linie
Platí pro národní referenční laboratoře a výzkumné instituce v oblasti veřejného zdraví, v souladu s pozicí WHO v oblasti NGS.
Řešení genomického dohledu od společnosti Macro & Micro-Test podporují sekvenování celého genomu pro sledování virů, objasnění přenosového řetězce, monitorování variant a úpravu vakcinační strategie. Podporují manuální/automatizované pracovní postupy, zlepšují propustnost a reprodukovatelnost a umožňují laboratořím přejít z rutinního testování na pokročilý dohled, v souladu s důrazem WHO na posílení monitorování virové evoluce.

4.4 Hodnota integrovaných řešení
Společnost Macro & Micro-Test poskytuje kompletní diagnostická řešení pro detekci arbovirů a podporuje každou fázi zvládání ohnisek nákazy: nástroje pro rychlý screening pro zdravotnická zařízení v první linii, molekulární potvrzení pro přesnou diagnózu a možnosti analýzy celého genomu pro epidemiologický dohled. Díky vysoce výkonným testům, flexibilním pracovním postupům a platformám připraveným na automatizaci tato řešení umožňují laboratořím a systémům veřejného zdraví posílit připravenost a reakci na nově vznikající arbovirové hrozby po celém světě.
Reference
[1] Světová zdravotnická organizace. Laboratorní testování viru dengue: Prozatímní pokyny, duben 2025. Ženeva: Světová zdravotnická organizace; 2025.
[2] Technická poradní skupina pro Globální iniciativu WHO pro arbovirová onemocnění. Posilování globální připravenosti a reakce na hrozby arbovirových onemocnění: Výzva k akci. Lancet Infect Dis. 2026;26(1):15-17.
[3] The Lancet Microbe. Překonání dilematu diagnostiky horečky dengue. Lancet Microbe. 2025;6(7):101190.
Čas zveřejnění: 20. března 2026
