I. PřehledESMOSměrnice pro rok 2025
V srpnu 2025 organizace ESMO oficiálně vydala publikaci Časný a lokálně pokročilý nemalobuněčný karcinom plic: Klinická doporučení ESMO pro diagnostiku, léčbu a sledování, která byla publikována v předním onkologickém časopise Annals of Oncology. Jedná se o první komplexní aktualizaci od verze z roku 2017 a poskytuje mimořádně autoritativní referenční materiál pro onkology po celém světě.

Rakovina plic má celosvětově nejvyšší incidenci a úmrtnost ze všech malignit. Každý rok se objeví více než 2,2 milionu nových případů a přes 1,8 milionu úmrtí, což činí rakovinu plic hlavní příčinou úmrtí na rakovinu u mužů i žen. Nemalobuněčný karcinom plic (NSCLC) představuje přibližně 80–85 % všech pacientů s rakovinou plic. Vzhledem k této závažné situaci vnáší vydání směrnice z roku 2025 do klinické praxe nový vědecký impuls, přičemž aktualizace strategií testování biomarkerů je obzvláště důležitá.
II. Interpretace aktualizací klíčových pokynů
2.1 Testování biomarkerů: Od „volitelného“ k „nezbytnému“
Pokyny z roku 2025 představují zásadní strategickou úpravu týkající se testování biomarkerů. Pokyny výslovně uvádějí, že testování biomarkerů je nezbytné pro rozhodnutí o léčbě pacientů s NSCLC ve stádiu IB-III.“
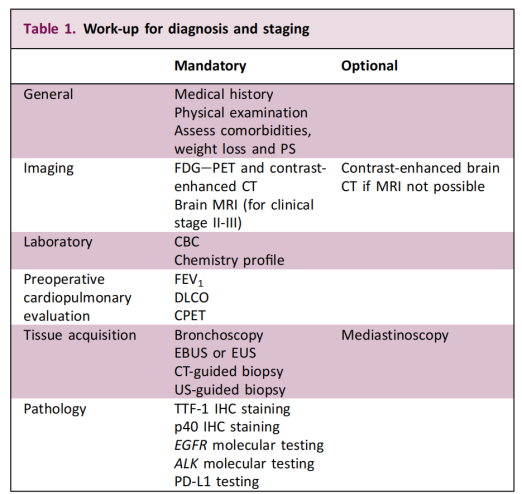
Toto doporučení rozšiřuje molekulární testování z jeho předchozího zaměření na pacienty s pokročilým onemocněním na případy v rané fázi, které lze resekovat. Hlavním cílem je identifikovat mutace genů řídicích orgánů a poskytnout vědecký základ pro personalizovanou a precizní léčbu. Pokyny rovněž zdůrazňují, že proveditelnost biopsie a diagnostický přístup by měl být určen multidisciplinárním týmem na základě charakteristik pacienta a nádoru.
Pokud jde o specifickou strategii testování, směrnice jasně doporučuje, aby genetické testování bylo provedeno před rozhodnutím o chirurgickém zákroku a aby zahrnovalo alespoň EGFR a ALK. Tento koncept „testování předem“ má hluboký klinický význam pro přesnou stratifikaci a personalizovanou léčbu časného stádia NSCLC – včasnost a přesnost výsledků testů přímo určují volbu následné adjuvantní terapie.
2.2 Průlomové terapeutické objevy v časném stádiu NSCLC s pozitivním driver-onkogenem
Pokyny z roku 2025 integrují důkazy z několika významných klinických studií s cílem stanovit jasnou a přesnou léčebnou cestu pro pacienty s NSCLC v časném stádiu s pozitivním testem driver-oncogene.
Pacienti s pozitivní mutací EGFR:Na základě průlomové studie ADAURA se pooperační adjuvantní osimertinib po dobu tří let stal globálním standardem péče o pacienty s delecemi EGFR exonu 19 nebo mutacemi L858R exonu 21. Studie ADAURA je mezinárodní, multicentrická, randomizovaná, kontrolovaná studie fáze III, která hodnotí účinnost a bezpečnost adjuvantního osimertinibu u pacientů s kompletně resekovaným NSCLC stadia IB-IIIA s mutací EGFR. Studie prokázala, že osimertinib významně zlepšil jak přežití bez onemocnění, tak celkové přežití ve srovnání s placebem, čímž se osimertinib stal novým standardem péče pro tuto populaci. Explorativní analýzy studie ADAURA však ukázaly, že přibližně 36 % předčasného ukončení léčby bylo způsobeno nežádoucími účinky a dalších 31 % bylo způsobeno rozhodnutím pacienta. Toto zjištění zdůrazňuje potřebu přesného vstupního testování před léčbou, aby se zajistilo, že cílená léčba bude podávána pacientům, kteří mohou mít trvalý přínos.
ALK-pozitivní pacienti:Na základě studie ALINA je nyní standardem péče pooperační adjuvantní léčba alektinibem po dobu dvou let. V primární analýze randomizované otevřené studie ALINA fáze III prokázal alektinib výrazný přínos v přežití bez onemocnění u populace pacientů ve stadiu II-IIIA s poměrem rizik 0,24. Aktualizovaná data ze studie ALINA prezentovaná na kongresu ESMO 2025 ukázala, že po ≥3 letech sledování zůstal přínos alektinibu z hlediska přežití bez onemocnění „trvalý a klinicky významný“ s poměrem rizik 0,36 u populace pacientů ve stadiu II-IIIA. Nejnovější hlášená celková míra přežití po 4 letech dosáhla 98,4 %, míra přežití bez onemocnění po 4 letech byla 75,5 % a zlepšilo se i přežití bez onemocnění centrálního nervového systému, a to bez jakýchkoli nových bezpečnostních signálů. Tato robustní data dále potvrzují adjuvantní léčbu alektinibem jako standard péče po resekci ALK-pozitivního NSCLC a podtrhují význam přesného testování k identifikaci těchto pacientů.
Volba testovací metody:Pokyny ESMO z roku 2025 výslovně uvádějímultiplexní RT-PCR panelové testyspolu s NGS na bázi RNA, IHC a FISH jako jedním z doporučených technických přístupů pro detekci fúze ALK. To naznačuje, že základním požadavkem směrnice je provádět testování k podpoře klinických rozhodnutí, spíše než nařizovat specifickou testovací platformu. U produktů RT-PCR zaměřených na detekci EGFR a ALK poskytuje tato flexibilní testovací strategie silné zdůvodnění pro jejich použití v klinické praxi založené na směrnicích.
III. Technická řešení pro přesné testování
Pokyny z roku 2025 posouvají testování do fáze předoperačního rozhodování, což zvyšuje laťku přesnosti, citlivosti a dostupnosti testů. Dva níže popsané detekční produkty založené na RT-PCR přesně splňují požadavky pokynů z technického hlediska.
3.1 Souprava pro detekci mutací EGFR – vylepšená technologická platforma ARMS
Základní technologieVylepšená technologie ARMS umožňuje specifickou amplifikaci mutantních sekvencí s nízkým výskytem na pozadí s vysokým obsahem divokého typu.
Tři technické záruky:
-Vylepšený ARMS → zlepšuje rozpoznávání mutací
-Enzymatické obohacení → štěpí pozadí divokého typu a obohacuje mutantní sekvence
-Teplotní blokování → potlačuje nespecifickou amplifikaci
VýkonCitlivost1% frekvence mutantních alel
Kontrola kontaminaceVestavěná interní kontrola + enzym UNG zabraňují kontaminaci
Doba vyřízeníProvoz v uzavřené trubici, přibližně120 minut
Kompatibilita vzorků:Tkáň/tekutá biopsievzorky → řeší požadavek „testování předem“
Krytí:45 mutacív exonech 18-21 EGFR, přesně odpovídající oblastem zvýrazněným dle pokynů (delece v exonu 19 a exon 21 L858R)
Klinické použitíPřímo řídí terapii EGFR-TKI
3.2 Sada pro detekci fúze MMT EML4-ALK – roztok pro detekci fúze na bázi RNA

-Technologická platformaRT-PCR na bázi RNA – nabízí inherentní výhody oproti metodám založeným na DNA pro detekci fúze
-Výhoda založená na RNAPřímo detekuje exprimované fúzní transkripty, čímž účinně zabraňuje falešně negativním výsledkům
-Studijní důkazyU fúzí ALK s nízkým výskytem je RT-PCR výrazně spolehlivější než testy založené na DNA.
-CitlivostDetekuje fúze až do20 kopií na reakci
-Pokrytí variantKryty12 běžných fúzních variant EML4-ALK(včetně varianty 1 ~33 %; varianty 3a/3b dohromady ~29 %)
-Provoz a kontrola kontaminaceUzavřená zkumavka, ~120 minut; vestavěné procesní kontroly + enzym UNG zabraňují falešným výsledkům
-Kompatibilita přístrojůKompatibilní s různými běžnými přístroji pro real-time PCR
-Zarovnání vodicích liniíVysoce konzistentní s pokyny ESMO
IV. Soulad mezi testy a doporučeními směrnice
Tyto dva detekční produkty jsou v následujících klíčových aspektech vysoce shodné s doporučeními ESMO 2025 pro časný a lokálně pokročilý nemalobuněčný karcinom plic:
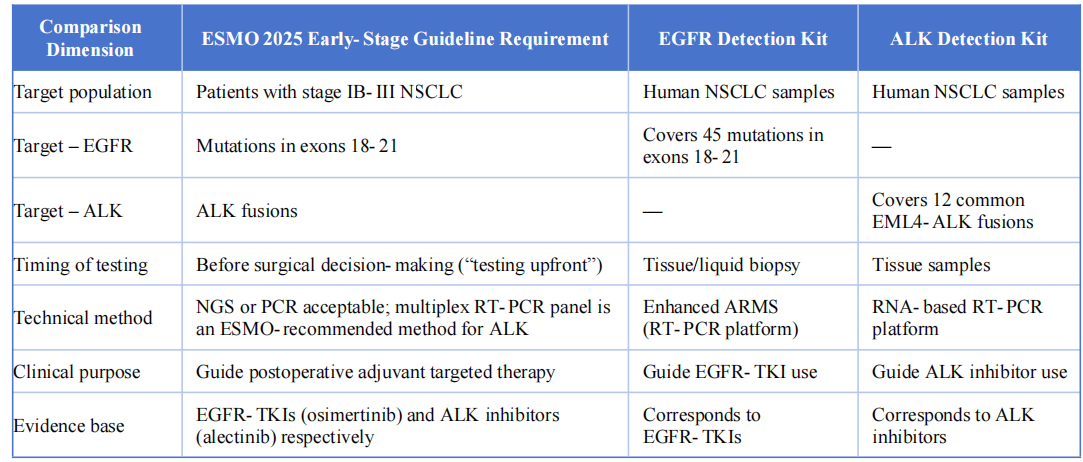
V. Závěr
Směrnice ESMO 2025 pro časný stadium NSCLC otevírá novou éru přesné diagnostiky a léčby, zaměřené na „předběžné testování, přesné cílení a optimalizace léčby.„Souprava pro detekci mutací EGFR a sada pro detekci fúze MMT EML4-ALK splňují požadavky směrnice na cíle, načasování a přesnost prostřednictvím odlišných technických postupů.“
Souprava EGFR využívá vylepšenou technologii ARMS pro vysoce citlivou detekci cílených mutací v omezeném množství vzorků a podporuje tkáňovou i tekutou biopsii, což umožňuje „testování předem“.
Souprava ALK je založena na RNA RT-PCR a nabízí oproti DNA metodám detekce fúzí výhodu. Je v souladu s doporučením ESMO pro multiplexní RT-PCR panely pro testování ALK.
Tyto dva produkty společně tvoří přesné testovací řešení, které je v souladu s pokyny ESMO 2025 a podporuje personalizovanou adjuvantní terapii pro NSCLC v raném stádiu.
Reference:
- Zer A, Ahn MJ, Barlesi F a kol. Časný a lokálně pokročilý nemalobuněčný karcinom plic: Klinická směrnice ESMO pro diagnostiku, léčbu a následné sledování. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Čas zveřejnění: 6. května 2026

